Les applications des méthodes non animales
Des exemples pratiques / concrets
La panoplie des outils et méthodes ne recourant pas à l’animal s’étoffe. Ainsi, les domaines pour lesquels ces méthodes s’appliquent sont de plus en plus variés.
Ces nouvelles technologies et approches méthodologiques offrent non seulement la possibilité d’une meilleure compréhension de nombreuses pathologies humaines, mais aussi une meilleure évaluation des effets toxiques de substances chimiques sur le métabolisme humain.
Dans l’objectif notamment de découvrir de nouveaux traitements et mettre sur le marché des substances et produits plus fiables, les méthodes non-animales représentent un intérêt certain pour la santé humaine. Elles ouvrent même une nouvelle ère dans ce domaine.
 Découvrons ensemble quelques-unes des très nombreuses applications de ces méthodes innovantes.
Découvrons ensemble quelques-unes des très nombreuses applications de ces méthodes innovantes.
Modèle oculaire constitué à partir de cellules souches pour effectuer les tests d’irritation
Au sein de l’Union Européenne des tests oculaires sont effectués avec des animaux en tant que sujet (principalement des lapins) pour tester des produits chimiques tels que des pesticides ou des médicaments. Ces tests d’irritation cutanée, appelés test de Draize, consistent à déposer dans les yeux de l’animal une substance pendant au minimum une heure et de détecter les éventuels risques d’irritation au cours des jours qui suivent.
Dans l’optique de diminuer ce fardeau animal, la norme ISO 10993 – 23:2021 valide les méthodes de reconstruction d’épiderme humain (RhE) qui imitent la fonction barrière de la couche cornée de l’humain pour prédire la réaction des tests d’irritation du tissu cutané.
Dans la même perspective, les méthodes de test d’irritation oculaire (TIO) tels qu’EpiOcular, SkinEthic avec épithélium cornéen humain (HCE), le LabCyte CORNEA-MODEL24 et le MCTT HCE contribuent à rester fidèle à l’organisation 3D de l’épithélium cornéen afin d’identifier correctement des produits chimiques ne relevant d’aucune classification pour l’irritation oculaire ou les lésions oculaires graves.
Elles suivent d’ailleurs la ligne directrice 492 de l’OCDE mise à jour en 2023.

Les organoïdes sur puce pour étudier les tumeurs cancéreuses
Développé par l’Institut FEMTO-ST de l’université de Franche-Comté, le projet 3D Glimpse vise à créer une tumeur sur puce afin de mieux comprendre et traiter le glioblastome, un cancer très agressif avec une survie moyenne d’un an après diagnostic. Dans cette puce, on va chercher à créer un gel représentant le micro-environnement tumoral via l’utilisation de différents types de cellules humaines qui s’organisent en 3D afin de former des micro-vaisseaux. Ceux-ci seront perfusés pour mimer le flux sanguin afin d’étudier le transport et l’efficacité de nouveaux nano-médicaments. Le projet mené par le Dr Agathe Figarol et son équipe a reçu le prix Descroix-Vernier EthicScience 2023 dans la catégorie Innovation.
Les recherches menées par le Dr Julien Marie et Sophie Léon du Centre de Recherche en Cancérologie de Lyon (CRCL) ont permis la mise au point d’une méthode alternative à l’animal qui se fonde sur le maintien en vie de la tumeur du patient après chirurgie ou biopsie. La méthode permet la conservation de l’intégrité biologique et des interactions cellulaires au sein du tissu, y compris du système immunitaire.
Cette approche ex-vivo novatrice présente une rapidité et une facilité de mise en œuvre, ainsi qu’une haute reproductibilité. Validée et publiée sur trois types de cancer (sein, poumon, mélanome), cette technologie ex-vivo a pour objectif d’être adaptée à d’autres cancers, notamment ceux de mauvais pronostic comme le pancréas, et aux formes pédiatriques pour accélérer la mise à disposition de nouveaux acteurs thérapeutiques.
Visant à être proposée à l’ensemble des chercheurs en biologie du monde académique et industriel, la technologie des deux chercheurs ont également été récompensés par en 2023 par le Prix Descroix-Vernier EthicScience dans la catégorie Développement et Applicabilité.
Le foie sur puce pour l’analyse de la toxicité de molécules à visée thérapeutique
Plus de 90% des molécules testées sur des animaux échouent lors des premiers essais cliniques chez l’humain. 30% de ces molécules rejetées sont liées à la toxicité.1
Face à un tel taux d’échec, les chercheurs et les industriels s’accordent sur l’urgence et l’importance de développer des modèles in vitro avancés, de type organoïdes à partir de cellules humaines.
Le foie est un organe central dans l’étude des potentiels risques toxiques des substances chimiques. En effet, organe annexe à l’intestin grêle et tissu parmi les plus importants de l’organisme, le foie assure de nombreuses fonctions métaboliques et régulatrices dont la transformation et l’assimilation des nutriments et des xénobiotiques (molécules étrangères à l’organisme dont les médicaments) absorbés par le tractus digestif, et par conséquent des fonctions de détoxification.
Dès lors, les organoïdes sur puce de foie représentent des techniques de premier plan pour l’étude toxicologique des substances chimiques dont celles à visée thérapeutique.
Pour contribuer à la résolution du fort taux d’échec des molécules candidates, des entreprises, telles que la société américaine Emulate, proposent aux chercheurs des foies sur puce dans le cadre des études en amont de toxicité de molécules2 pour une validation à visée thérapeutique avec des études d’évaluation de performance et d’analyse économique à l’appui.3
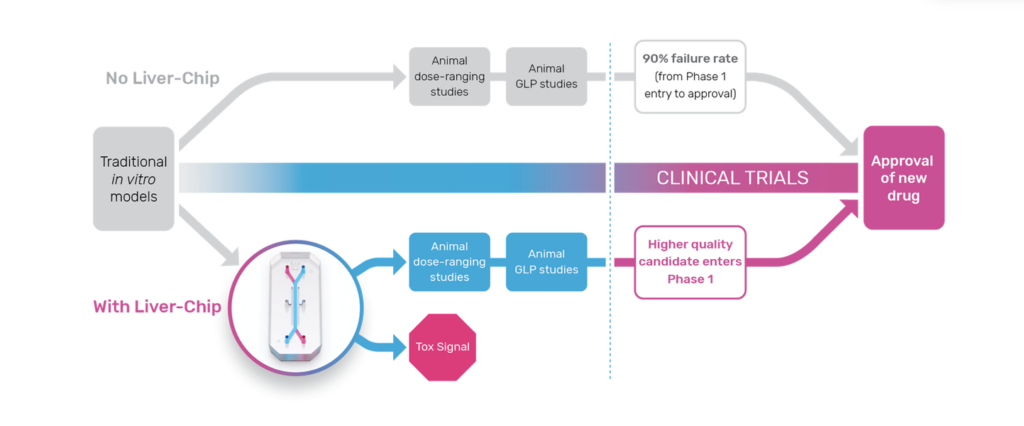
Schéma Emulate
Au niveau français, des projets de foie sur puce voient également le jour tels que le projet MimLiveronChip développé dans le cadre de l’anr (agence nationale de recherche).
MimLiveronChip est définie et conçue comme une Plateforme biomimétique de Foie sur puce.
Le projet a été développé pour recréer l’analyse du métabolisme du foie et de la toxicité des xénobiotiques. MimLiveronChip cherche plus particulièrement à explorer les effets du microenvironnement mécanique ou biochimique influençant l’ouverture de la monocouche du foie, afin de pouvoir la générer ou au contraire de l’altérer.
Le projet est fondamentalement pluridisciplinaire s’appuyant sur la collaboration étroite entre quatre équipes d’expertises complémentaires : ingénierie tissulaire hépatique à différente échelles (UMR UTC-CNRS Biomécanique et Bioingénierie), microsystèmes et biologie des cellules endothéliales (SMMIL‑E – UMI CNRS), pour la partie académique, PME leader dans les équipements pour la microfluidique (Fluigent) ainsi qu’une start-up développant des méthodes in vitro pour l’évaluation des xénobiotiques (HCS Pharma).4
Les Systèmes Micro-Physiologiques multi-organes pour prédire la biodisponibilité chez l’humain
Un système micro-physiologique (MPS pour MicroPhysiological System) est l’autre appellation de la technologie de l’organe sur puce. Les systèmes micro-physiologiques multi-organes ont ainsi la particularité de connecter plusieurs organes entre eux et de reproduire à la fois leurs fonctions physiologiques respectives, mais aussi leurs interactions.
En 2023 la FDA (Food and Drug Administration) et la société CN Bio ont confirmé un second partenariat pour de nouvelles recherches afin d’évaluer les Systèmes Micro-Physiologiques (MPS) multi-organes et leurs applications à l’aide du système PhysioMimix.
Le modèle PhysioMimix est un modèle intestin/foie qui recrée in vitro la structure et la fonction de ces tissus humains et leur interaction fluidique, reproduisant de manière unique l’effet combiné de la perméabilité intestinale et du métabolisme faisant du dispositif un système de choix pour la prédiction de la biodisponibilité orale humaine.
Le système est étudié pour améliorer l’estimation préclinique de la biodisponibilité des médicaments humains par rapport aux modèles animaux. En effet, malgré le caractère encore dominant des modèles animaux lors de l’estimation de la biodisponibilité, les études montrent que ces derniers sont des modèles peu prédictifs, notamment en raison des différences physiologiques et métaboliques inhérentes.
Pour rappel, la biodisponibilité correspond à la vitesse et à l’importance du passage du principe actif (médicament ou métabolite) dans la circulation générale, gagnant ainsi le site d’action.
Prédire avec précision cette biodisponibilité chez l’humain au cours du développement préclinique est crucial ; paramètre critique pour les développeurs de médicaments et les agences de réglementation afin d’établir des doses sûres et efficaces dans la clinique.
La combinaison des méthodes in omic avec les organoïdes pour dépister le développement des troubles du spectre autistique
Les organoïdes sont des reproductions in vitro d’organes à base de cellules souches. Ils ont pour avantage de reproduire la même structure 3D des organes voulus. Grâce à cette configuration tridimensionnelle, on obtient des fonctionnalités et des caractéristiques plus proches du vivant et donc de l’humain.
Les chercheurs de l’Institut de Biotechnologie Moléculaire (IMBA) d’Autriche et l’école polytechnique fédérale de Zurich (ETH) ont eu l’idée de créer un organoïde du cerveau afin de dépister le développement de l’autisme.
Dans l’objectif de mettre en exergue les troubles autistiques via cet organoïde, les chercheurs utilisent la génomique. La génomique est une sous branche des méthodes dites in omic basées sur l’étude de la composition protéique des cellules et de leurs activités. La génomique consiste à analyser plus particulièrement le génome (l’ensemble du matériel génétique d’un individu ou d’une espèce) en cherchant les gènes altérés ou les activités anormales des protéines au sein d’un organisme entier ou d’un organe.
Aujourd’hui, et afin de contribuer à une détection précoce des troubles autistiques, les chercheurs de l’IMBA et de l’ETH ont donc créé, à partir de l’outil CRISPR cas 9, le système CRISPR-Human Organoïds-Single-Cell RNA (CHOOSE) afin de visualiser les gènes impliqués dans le spectre autistique sur la base de 36 gènes différents identifiés.
Pour rappel, CRISPR cas 9 est un outil révolutionnaire dans la génétique depuis 2012 et pour lequel les chercheures Emmanuelle Charpentier et Jennifer A. Doudna ont reçu le prix Nobel de chimie 2020. Cette technologie, communément appelée ciseaux génétiques, permet en effet d’effectuer des modifications génétiques précises sans endommager l’ADN.
Ainsi, par la technologie de CRISPR cas 9, les chercheurs ont pu modifier les gènes identifiés afin de les rendre plus visibles dans l’organoïde de cerveau en utilisant la fluorescence. La fluorescence permet de mettre en évidence les gènes transcrits en ARN allant du bleu au rouge correspondant à la mutation du gène impliqué dans le spectre autistique.
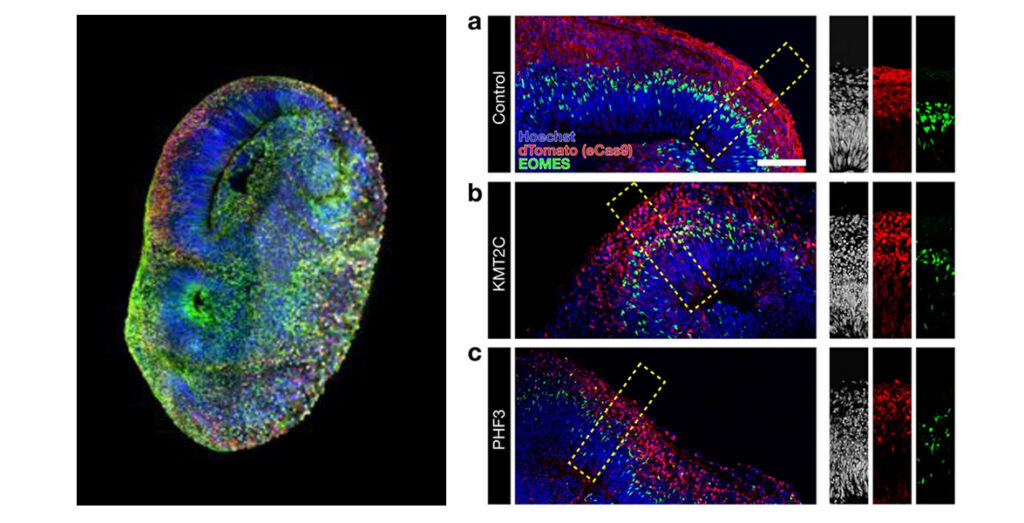
Gauche ©Knoblich Lab / IMBA-IMP Graphics I Extrait article Sept. 2023, GEN Image confocale d’un système de mosaïque organoïde de cerveau humain CHOOSE (CRISPR-human organoids-scRNA-seq) montrant des cellules porteuses d’une mutation en rouge. Moitié droite : une représentation en mosaïque de différentes couleurs représentant des cellules individuelles, chacune portant une mutation dans un gène de l’autisme de haute fiabilité. Droite © Li, C., Fleck, J.S., Martins-Costa, C. et al. Single-cell brain organoid screening identifies developmental defects in autism. Nature 621 a‑c, images confocales montrant une coloration immunohistochimique sur des organoïdes âgés de 60 jours perturbés par des gènes individuels. dTomato marque les cellules induites par eCas9.
A l’aide de cette combinaison de méthodes, le CRISPR-Human Organoïds-Single-Cell RNA (CHOOSE) rend possible d’une part de déterminer l’effet de la mutation d’un gène ou plusieurs sur le développement de la cellule, et d’autre part de visualiser la quantité de gènes impliqués permettant une meilleure identification du spectre autistique.5
La simulation de mécanismes neurologiques pour mieux guider la chirurgie de l’épilepsie
L’épilepsie touche 50 millions de personnes dans le monde, ce qui en fait l’une des maladies neurologiques les plus répandues. Ce trouble se caractérise par des crises récurrentes de tremblement partiel de l’ensemble du corps pouvant aller jusqu’à la convulsion. Il en résulte de décharges électriques excessives dans un groupe de cellules cérébrales.6
On estime que 70% des personnes atteintes pourraient ne pas subir les crises avec des médicaments anti-épileptiques. Dans le cas contraire, la chirurgie du cerveau est le seul moyen d’éviter définitivement les troubles causés par l’épilepsie. Malgré les progrès techniques, le taux de réussite de cette chirurgie ne s’est pas beaucoup amélioré et reste autour de 50 %.7
Le projet Epinov (EPilepsy Surgery Management And ProgNOsis Using Virtual Brain Technology) a pour objectif à la fois de mieux analyser le bilan préchirurgical des épilepsies résistantes aux médicaments, et de mieux guider les stratégies chirurgicales.
Epinov repose pour se faire sur une technologie de simulation cérébrale neuro-informatique : un cerveau virtuel développé par Viktor Jirsa, directeur de l’Institut de Neurosciences des Systèmes (Marseille) en collaboration avec le Pr Fabrice Bartolomei. Ce cerveau virtuel vise à améliorer significativement la visualisation des réseaux épileptogènes grâce notamment aux données de 175 patients.
Impliquant 11 centres de chirurgie de l’épilepsie en France, les travaux d’Epinov ont débuté en janvier 2018 et se terminent en décembre 2023.8 9
L’aide de la bio-impression 3D — 4D pour traiter le cancer du sein
En 2020, dans le monde, 2,3 millions de femmes ont été recensées avec le cancer du sein.10
En France, le cancer du sein est le cancer le plus fréquent chez la femme avec 60 000 nouveaux cas par an11 ; ce qui constitue le plus grand nombre de nouveaux cas sur l’ensemble des cancers. Le cancer du sein est une croissance incontrôlée de cellules mammaires. Cet amas de cellules est une tumeur.
Au cours de sa thèse, le doctorant Théo Desigaux a réussi à reconstituer, à partir d’un échantillon d’une patiente atteinte d’un cancer du sein et via la bio-impression 3D, la tumeur,12 dans l’objectif notamment d’étudier la tumeur directement sans impacter la patiente et de pouvoir avoir un traitement adapté. Cette reconstitution lui a valu de recevoir, en 2021, le prix Fondation ARC.13
On estime que 40% des personnes atteintes du cancer du sein doivent subir une ablation totale du sein, une mastectomie. Celle-ci peut s’avérer traumatisante. Ainsi, la reconstruction mammaire fait partie intégrante de la prise en charge. Le projet Seno-Print14 cherche à améliorer la reconstruction mammaire en développant une bio impression 3D de prothèses biologiques personnalisées. Ces prothèses bio-imprimées devraient s’adapter à la physiologie naturelle du sein, avec l’objectif de limiter le nombre d’interventions supplémentaires relatives à l’entretien et la durabilité de la prothèse.15
L’aide de la bio-impression 3D dans la production de vaccin viral
Il existe différents types de vaccins. Mais tous ont pour objectif de provoquer une réaction immunitaire de l’organisme. Celle-ci va permettre d’entraîner le corps à combattre la maladie inoculée. Le vaccin à ARN messager va chercher à produire lors de sa traduction au sein de la cellule une protéine sélectionnée et modifiée l’agent infectieux. Cette méthode fonctionne très bien pour les infections virales. Elle a aussi pour avantage de n’utiliser aucun animal lors de sa conception.16 Le vaccin est produit par synthèse chimique. De plus, produire l’ARN via la bio-impression a pour intérêt de travailler sur des quantités plus grandes et plus rapidement. Ce qui est très pratique lors d’épidémie. Elle s’utilise déjà pour la fièvre jaune notamment.17
L’aides des méthodes non-animales notamment in silico sur les maladies cardiaques
Le Centre commun de Recherche (JRC) et la Commission européenne ont établi un rapport technique sur les avancées du modèle non-animal dans la recherche biomédicale à propos des maladies cardiovasculaires.18 Il y a beaucoup d’échecs de thérapie impliquant des animaux et cherchent donc à développer de nouvelles méthodes plus efficaces et moins coûteuses. En effet l’utilisation d’animaux se retrouve être principalement des cochons ou des moutons au vu de leur cœur semblable aux nôtres.
Par exemple, les Cardiomyopathies sont causées par la présence d’anomalies dans la structure et la fonction du myocarde. Il est nécessaire de créer artificiellement l’anomalie cardiaque chez l’animal, ce qui est très différent du développement d’une maladie chez l’humain.
Ces méthodes comprennent 3 grands domaines d’application dans la recherche des maladies cardiaques, le développement de thérapie, son mécanisme et son diagnostic. Les maladies identifiées à ces méthodes concernent 22% des procédures d’interventions chirurgicales et 25% des maladies des valves cardiaques.
Sur les 449 méthodes sélectionnées dans le rapport du JRC, la méthode in silico ressort du lot avec environ 50% des techniques validées. Grâce à celle-ci, il est possible d’étudier les propriétés physiques de la circulation sanguine dans le système cardiovasculaire via une approche de dynamique des fluides tout en s’adaptant aux différentes pathologies cardiaques. Il est aussi possible de simuler le mouvement des muscles du myocarde. Cette approche est mise en avant car elle permet de prédire les résultats cliniques et d’aider à sa conception, d’étayer les preuves d’efficacité, d’identifier les patients les plus pertinents à étudier et prédire la sécurité des produits.
Des méthodes ex vivo sont aussi intéressantes dans la compréhension de mécanismes biomécanique des pathologies cardiaques tels que pour l’anévrisme. Lors d’opérations, le chirurgien retire la section d’artère affectée et suture un greffon pour l’étudier. Cet aspect est important pour une analyse plus approfondie des maladies cardiovasculaires.
Les modèles synthétiques humains et animaux et les interfaces virtuelles pour la formation clinique et chirurgicale
L’évolution technologique au sein de l’éducation donne lieu progressivement à de nouvelles pratiques et méthodes de formation par le biais de dispositifs de simulation destinés tant aux étudiants en médecine humaine que vétérinaire. En effet, la formation médicale et la formation chirurgicale en particulier sont basées sur l’apprentissage de la théorie et la mise en pratique, dans certains cas sur l’animal, particulièrement le cochon en chirurgie, avant d’être poursuivie par l’expérience clinique acquise via le contact direct des étudiants avec les patients.
En France en 2016, 34 000 animaux ont été tués à des fins éducatives. La même année, les universités et centres de formation britanniques n’ont utilisé que 1 422 animaux. En France, le nombre d’animaux utilisés pour l’enseignement et la formation a augmenté de 31 % depuis 2010.

Modèles synthétiques Syndaver
Les modèles synthétiques reproduisent l’anatomie humaine et animale de manière très précise, y compris les muscles, les tendons, les veines, les artères, les nerfs et les organes individuels. Fabriqués à partir de composites complexes, les modèles produits reproduisent les propriétés mécaniques, physico-chimiques, thermiques, des tissus vivants concernés. Les modèles peuvent saigner et respirer, utilisent des centaines de muscles, d’os, d’organes et de vaisseaux remplaçables.
Les travaux sur cette technologie de modèles synthétiques ont été lancés en 1993 à l’Université de Floride (USA). Les matériaux et modèles développés depuis peuvent remplacer l’utilisation des animaux dans l’étude de dispositifs médicaux, la formation clinique et la simulation chirurgicale, tant dans le domaine humain que vétérinaire, mais aussi dans l’évaluation des produits de consommation et les tests balistiques, comme le propose la société Syndaver.
Des tables / interfaces virtuelles au rendu hyper réaliste sont obtenues grâce à des données issues de l’imagerie médicale fusionnées avec des données anatomiques. Offrant une véritable bibliothèque anatomique numérique 3D, ces dispositifs sont enrichis par des collections de scanners cliniques et des centaines de scénarios afin d’appréhender la complexité de cas réels dans une grande variété d’environnements. Ces patients virtuels atteints de symptômes évoluant dans le temps basé sur des algorithmes physiologiques, fournissent des expériences de simulation immersive pertinentes représentant un environnement sûr et interactif pour le développement du raisonnement clinique et des compétences décisionnelles.
Les simulateurs, tel que le dispositif BodyInteract, sont utilisés dans le processus d’enseignement de différentes matières cliniques telles que la neurologie, la cardiologie, l’obstétrique, la pédiatrie, les maladies infectieuses, etc.
Crédit : iStock — DepositPhotos — Comité scientifique Pro Anima
Logo : Atelier Pincel
- Emulate. https://emulatebio.com/toxicology/
- Emulate. https://emulatebio.com/toxicology/
- Ewart, L., Apostolou, A., Briggs, S.A. et al. Performance assessment and economic analysis of a human Liver-Chip for predictive toxicology. Commun Med 2, 154 (2022).
- ANR, Projet MIMLIVERonChip. https://anr.fr/Projet-ANR-19-CE19-0020
- Li, C., Fleck, J.S., Martins-Costa, C. et al. Single-cell brain organoid screening identifies developmental defects in autism. Nature 621, 373 – 380 (2023).
- OMS, Epilepsie, 2023. https://www.who.int/fr/news-room/fact-sheets/detail/epilepsy
- 3DS Dassault Système ; Le Living Brain dans la Chirurgie de l’Epilepsie. https://www.3ds.com/fr/insights/living-brain
- INS, Epinov projet, Improving EPilepsy Surgery Management And ProgNOsis Using Virtual Brain Technology. https://ins-amu.fr/epinov
- ANR, Projet Epinov, Improving EPilepsy Surgery Management And ProgNOsis Using Virtual Brain Technology. https://anr.fr/ProjetIA-17-RHUS-0004
- OMS, Cancer du sein. https://www.who.int/fr/news-room/fact-sheets/detail/breast-cancer#:~:text=En%202020%2C%20on%20a%20recens%C3%A9,du%20sein%20dans%20le%20monde.
- Santé Publique France, Cancer du sein. https://www.santepubliquefrance.fr/maladies-et-traumatismes/cancers/cancer-du-sein
- Thèses France, Théo Desigaux, Décrypter le dialogue des cellules de tumeur du sein avec leur écosystème, après radio/chimiothérapie, en utilisant des technologies de bio impression. https://www.theses.fr/s345537
- Fondation ARC, Journées Jeunes Chercheurs 2021. https://www.fondation-arc.org/JJC2021
- Université Côte d’Azur ; Projet Seno-print. https://imredd.fr/projet/seno-print/
- Fond avenir, Projet Seno-print, 2021. https://www.fonds-aveni.fr/senoprint-developpement-bio-impression-3d-protheses-biologiques-reconstruction-mammaire-apres
- INRAE, Avantages, désavantages, risques… Ce qu’il faut savoir sur les vaccins à ARN , 2020. https://www.inrae.fr/actualites/avantages-desavantages-risques-ce-quil-faut-savoir-vaccins-arn
- Yi, HG., Kim, H., Kwon, J. et al. Application of 3D bioprinting in the prevention and the therapy for human diseases. Sig Transduct Target Ther 6, 177 (2021). https://www.nature.com/articles/s41392-021 – 00566‑8#Sec19
- Rapport JRC, Advanced Non-animal Models in Biomedical Research, Cardiovascular diseases, 2022. https://publications.jrc.ec.europa.eu/repository/handle/JRC130702


